轉(zhuǎn)載 | 限制藥物研發(fā)中的動(dòng)物試驗(yàn)?虛驚一場過后的思考
來源:同寫意
時(shí)間:Oct,2022
瀏覽次數(shù):2011次
醫(yī)藥研發(fā)中的動(dòng)物使用將會(huì)受到嚴(yán)格限制。近期,美國參議院通過了一項(xiàng)與醫(yī)藥工業(yè)相關(guān)的重要法案,《FDA現(xiàn)代化法案2.0》。該法案意在取消對新藥研發(fā)中進(jìn)行動(dòng)物試驗(yàn)和取消生物仿制藥的動(dòng)物試驗(yàn)的強(qiáng)制性要求。
需要注意,美國FDA每年的財(cái)務(wù)預(yù)算是由美國國會(huì)批準(zhǔn),而不是由總統(tǒng)批準(zhǔn)。既然上述法案已經(jīng)獲得了美國參議院一致通過,預(yù)計(jì)美國眾議院也會(huì)順利過關(guān)。所以,限制美國醫(yī)藥研發(fā)中的動(dòng)物使用估計(jì)已成為定局。
長期以來,動(dòng)物試驗(yàn)一直作為臨床前藥理研究和安全性評價(jià)的重要手段,是什么原因推動(dòng)了此次法案的順利通過?此次動(dòng)物試驗(yàn)的取消意味著什么?我們通過研究動(dòng)物試驗(yàn)替代技術(shù)發(fā)展歷史,政治經(jīng)濟(jì)因素,及替代技術(shù)的最新進(jìn)展或許不難找到答案。
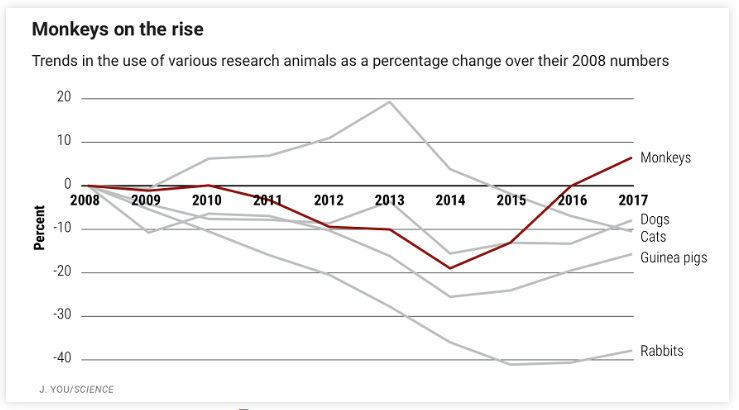
藥物安全性評價(jià)是藥物開發(fā)的重要環(huán)節(jié),涉及識別化學(xué)品和生物制品對人類、植物、動(dòng)物和環(huán)境的不良事件(AE)。而臨床前安全性評估,是防止有毒藥物進(jìn)入臨床試驗(yàn)的必要條件。盡管如此,安全性問題仍然是導(dǎo)致藥物開發(fā)失敗的主要原因,占上市后藥物退出的三分之二和臨床試驗(yàn)期間失敗的五分之一。因此,對毒性的準(zhǔn)確估計(jì)是確保藥物安全的必要前提,也有助于降低將新藥推向市場的開發(fā)時(shí)間和成本。不可否認(rèn),實(shí)驗(yàn)動(dòng)物為醫(yī)學(xué)的發(fā)展和藥物的成功開發(fā)做出了重要貢獻(xiàn),同時(shí)也造成了動(dòng)物遭受了痛苦的肉體折磨和不必要的死亡。其實(shí),早在1959年英國動(dòng)物學(xué)家William Russell和微生物學(xué)家Rex Burch就提出了3R理論,通過用減少(Reduce),優(yōu)化(Refine),替代(Replace)三種方式來提高動(dòng)物福利和優(yōu)化實(shí)驗(yàn)設(shè)計(jì)來達(dá)到高效實(shí)驗(yàn)的目的。他們還提出了相對代替和絕對代替的概念,指出可利用低等動(dòng)物、高等植物、微生物方法和生化檢測的方法代替動(dòng)物測試,并富有遠(yuǎn)見性地提出充分開發(fā)組織培養(yǎng)的觀念。1978年英國生理學(xué)家David Symth主張將3R統(tǒng)稱為替代方法(Alternatives)。3R理論提出以來,開拓了人們?nèi)绾伍_展生命科學(xué)研究的思路,使得仁慈科學(xué)成為良好科學(xué)的前提,并激勵(lì)科學(xué)家開始研究各種替代技術(shù)開發(fā)。3R原則一直影響著世界各國有關(guān)實(shí)驗(yàn)動(dòng)物法規(guī)。目前,西方大多數(shù)國家的《實(shí)驗(yàn)動(dòng)物福利法》均引入了3R原則。中國科技部2006年發(fā)布了《關(guān)于善待實(shí)驗(yàn)動(dòng)物的指導(dǎo)性意見》。2019 年,美國環(huán)保署承諾將在2025年將動(dòng)物試驗(yàn)數(shù)量減少 30%,并在2035年前結(jié)束所有用于評估化學(xué)品對人類健康和環(huán)境風(fēng)險(xiǎn)的哺乳動(dòng)物試驗(yàn)。然而值得注意的是2035年的具體截止日期已從美國環(huán)保署(EPA)的2021年新技術(shù)方法(NAMs)工作計(jì)劃中刪除。藥物安全是新藥上市的主要挑戰(zhàn)。意外的毒性和副作用是候選藥物臨床試驗(yàn)失敗的主要原因之一,而上市后的藥物安全問題會(huì)導(dǎo)致患者不必要提高的發(fā)病率和死亡率。2008年至2017年間,美國FDA批準(zhǔn)了 321 種新藥。同期,F(xiàn)DA不良事件報(bào)告系統(tǒng)(FAERS)記錄了超過 1000 萬份AE報(bào)告,其中580萬份為嚴(yán)重報(bào)告,19%為與死亡相關(guān)的不良事件。僅以美國為例,不良事件給衛(wèi)生系統(tǒng)帶來負(fù)擔(dān),會(huì)導(dǎo)致每年200萬次住院,并將就診時(shí)間延長1.7至4.6 天。在現(xiàn)有的標(biāo)準(zhǔn)中,新藥在進(jìn)行臨床試驗(yàn)前必須在兩種動(dòng)物里檢驗(yàn)安全性,包括觀察潛在毒副作用以及不同劑量下的表現(xiàn)。對于一個(gè)全新的候選藥物,毒副作用存在不確定性,而在動(dòng)物中提前進(jìn)行體內(nèi)測試可幫助降低臨床試驗(yàn)藥品安全的不確定性,目前這仍然是進(jìn)入人體前的最后一道主要關(guān)卡。根據(jù)美國農(nóng)業(yè)部的新數(shù)據(jù),科學(xué)家去年使用了75825只非人類靈長類動(dòng)物(NHP)進(jìn)行研究,自2015年以來增長了22%,自2008年以來增長了6%。相比之下,美國農(nóng)業(yè)部記錄的貓,狗,兔子和其他動(dòng)物的數(shù)量都比十年前使用得更少。美國是全球?qū)嶒?yàn)猴使用數(shù)量最多的國家,2008年起每年的使用量穩(wěn)定在7萬只左右。據(jù)美國農(nóng)業(yè)部的實(shí)驗(yàn)猴使用數(shù)量報(bào)告顯示:2018-2019年,美國實(shí)驗(yàn)猴使用數(shù)量分別是70797只和68257只。在美國所消耗的實(shí)驗(yàn)猴中,有約一半是通過進(jìn)口獲得的,其中60%的進(jìn)口量來自于中國。2008-2017年美國各類實(shí)驗(yàn)動(dòng)物的使用數(shù)量的變化百分比(來源:Science)
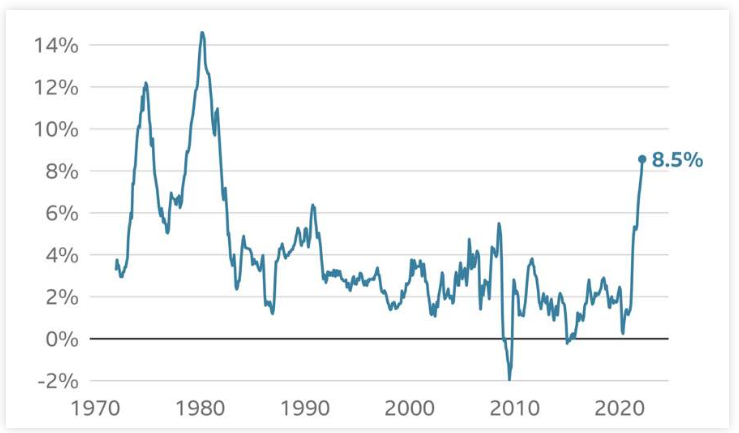
近幾年中國加大了對創(chuàng)新藥物研發(fā)的支持力度,中國的生物醫(yī)藥工業(yè)也開始了高速發(fā)展。這也造成了中國市場對實(shí)驗(yàn)動(dòng)物的大量需求。然而,由于動(dòng)物試驗(yàn)對動(dòng)物年齡有特定要求(猴類通常需要經(jīng)過三年的生長之后才能用于實(shí)驗(yàn)),加上其漫長的育種周期和低產(chǎn)出率,目前的猴源供應(yīng)未能跟上急速擴(kuò)大的市場需求。猴源短缺使實(shí)驗(yàn)猴的單價(jià)也從2017年的1.4萬元一路飆升至2022年的15萬元人民幣。此外近年幾乎所有的商業(yè)航空公司都拒絕運(yùn)送此類動(dòng)物,國外市場更可謂是“一猴難求”。由于目前沒有什么替代品可以減少非人類靈長類動(dòng)物的使用。因?yàn)樵囼?yàn)猴在生理和遺傳特征上與人類非常相似,除了用于藥物安全性評價(jià)外,非人類靈長類動(dòng)物(NHP)在其他許多生命科學(xué)領(lǐng)域也都充當(dāng)了重要的疾病動(dòng)物模型,這包括了傳染病、生殖生物學(xué)、再生醫(yī)學(xué)、老年疾病、神經(jīng)科學(xué)以及認(rèn)知和行為學(xué)研究。由于使用NHP進(jìn)行測試可以滿足各國監(jiān)管機(jī)構(gòu)對藥物安全評估的要求,特別在大分子藥物的安全性實(shí)驗(yàn)中,缺乏實(shí)驗(yàn)猴將極大的影響臨床藥物注冊的成功性。一路高漲的實(shí)驗(yàn)猴成本和等待時(shí)間,也成了制約各國藥企新藥研發(fā)進(jìn)度的關(guān)鍵,“天價(jià)猴哥”一時(shí)間成為了影響各國醫(yī)藥工業(yè)發(fā)展的戰(zhàn)略物資。對此,一直依賴從中國進(jìn)口實(shí)驗(yàn)猴的美國藥企開始擔(dān)憂起來了。2018年下半年,美國國家衛(wèi)生研究院(NIH)組織了兩次名為“非人靈長類動(dòng)物評估與分析”的會(huì)議。在會(huì)議上,進(jìn)口獼猴“卡脖子”的問題都是討論焦點(diǎn)。會(huì)上NIH動(dòng)物中心負(fù)責(zé)人Alphie Cisar提出,在獼猴的供給方面,需要盡量減少美國對中國試驗(yàn)猴進(jìn)口的依賴。同時(shí),美國國內(nèi)各類動(dòng)物權(quán)益保護(hù)組織的抗議之聲本來就不絕于耳,近兩年反對動(dòng)物試驗(yàn)情緒更是空前高漲,根據(jù)皮尤研究中心(Pew Research)2020年的一項(xiàng)民意調(diào)查發(fā)現(xiàn),破紀(jì)錄的有52%的美國人反對動(dòng)物試驗(yàn)研究。今年,美國通脹率陡增,達(dá)到40年來的新高,普通美國家庭生活成本危機(jī)加劇,在這個(gè)時(shí)候,推出這一有可能降低藥物研發(fā)成本的法案勢必能獲得廣泛支持。據(jù)Globe Newswire報(bào)道,此次現(xiàn)代化法案獲得了包括動(dòng)物健康行動(dòng)(Animal Wellness Action),人道經(jīng)濟(jì)中心(Center for Humane Economy)等近200個(gè)組織,醫(yī)學(xué)協(xié)會(huì),生物技術(shù)和患者倡導(dǎo)團(tuán)體的擁護(hù)。1970-2022年間美國通脹率同比變化(來源:美國勞動(dòng)統(tǒng)計(jì)局)
但是我們應(yīng)該看到,動(dòng)物試驗(yàn)仍然是不可缺少的藥物安全性評價(jià)手段之一。這次FDA雖然只是放松了對于臨床前動(dòng)物試驗(yàn)的強(qiáng)制性要求,但在美國工業(yè)界、動(dòng)物保護(hù)組織、政府和民眾看來都是一個(gè)多贏的選項(xiàng)。放寬監(jiān)管邊界有助于企業(yè)啟用新技術(shù),通過應(yīng)用替代技術(shù)優(yōu)化實(shí)驗(yàn)設(shè)計(jì)和提高質(zhì)量,從而一定程度上減少不必要的動(dòng)物試驗(yàn),有助于企業(yè)緩解資源緊缺帶來的成本壓力和時(shí)間損耗。取消動(dòng)物試驗(yàn),底氣從何而來?本次FDA法案的發(fā)起人之一,新澤西州參議員Cory Booker曾表示:“由于現(xiàn)代科學(xué)創(chuàng)新,將動(dòng)物毒理測試用于實(shí)驗(yàn)藥物安全性評價(jià)已經(jīng)變得越來越過時(shí)。當(dāng)科學(xué)上可靠的替代測試方法可用時(shí),這項(xiàng)立法將消除無數(shù)動(dòng)物的不必要痛苦。”確實(shí),這次新法案的通過,除了有部分政治和經(jīng)濟(jì)因素,有效替代動(dòng)物試驗(yàn)的技術(shù)也是必不可少的條件。隨著現(xiàn)代生物科學(xué)和信息技術(shù)的發(fā)展,為動(dòng)物試驗(yàn)的替代方法提供了理論基礎(chǔ)和技術(shù)支持,體現(xiàn)在充分利用先進(jìn)技術(shù)的精華并加以整合,如分子生物學(xué)、組學(xué)技術(shù)(基因組、蛋白組、代謝組、細(xì)胞組)、組織工程技術(shù)、干細(xì)胞技術(shù)、圖像分析、高通量試驗(yàn)、計(jì)算機(jī)模擬技術(shù)等,替代方法更復(fù)雜化、多元化,也更有邏輯性和更接近人作為整體的實(shí)際情況。由于各類動(dòng)物和人類數(shù)據(jù)可用性的提高,為人工智能的同步發(fā)展奠定了優(yōu)化數(shù)據(jù)的基礎(chǔ)。云計(jì)算是促進(jìn)“大數(shù)據(jù)”可視化和分析的資源的一個(gè)很好的例子,因?yàn)橐粋€(gè)用戶不需要下載和存儲(chǔ)大量數(shù)據(jù)。各類數(shù)據(jù)的存儲(chǔ)、管理、挖掘和可視化技術(shù)的發(fā)展至關(guān)重要,因?yàn)樾枰獙Σ粩喈a(chǎn)生的數(shù)據(jù)進(jìn)行分類和重新排列,以保持?jǐn)?shù)據(jù)使用的便捷性。這與藥物發(fā)現(xiàn)和化學(xué)安全性測試相互關(guān)聯(lián),因?yàn)樵絹碓蕉嗟目捎脭?shù)據(jù)需要“符合目的”的安全性和有效性評估工具,這將大大提高了提交給監(jiān)管部門所需數(shù)據(jù)的數(shù)量和質(zhì)量。多種新技術(shù)出現(xiàn)也催化了研發(fā)思維的突破性轉(zhuǎn)變,出現(xiàn)了“有害結(jié)局路徑”(AOP)為代表的新型毒理研究范式,從傳統(tǒng)的毒理學(xué)測試轉(zhuǎn)變到更機(jī)器化和數(shù)據(jù)驅(qū)動(dòng)的范式,最終建立疾病“地圖”和計(jì)算機(jī)方法(In silico),以及體外測試方法(In Vitro),并產(chǎn)生用于填補(bǔ)空白的 AI 衍生數(shù)據(jù)。最終目標(biāo)通過更多機(jī)器和人類相關(guān)數(shù)據(jù)來闡明生物學(xué)途徑,從而提高理解能力。英國的AI制藥企業(yè)Exscientia在2014年就開始進(jìn)行數(shù)據(jù)積累,最終收集了1萬多種化學(xué)物質(zhì)。然后利用AI系統(tǒng)對數(shù)據(jù)庫中的化學(xué)物質(zhì)進(jìn)行了86萬次的測試,其繪制的分子結(jié)構(gòu)與特定毒性類型之間的關(guān)系,很多之前并不為人知,比如可能對眼睛、皮膚或DNA造成的影響。研究人員還對不同化學(xué)性質(zhì)和毒理性質(zhì)的物質(zhì)進(jìn)行分組,然后以組內(nèi)某一物質(zhì)的毒性為參照,推測其他物質(zhì)的毒性。再與這些其他物質(zhì)在數(shù)據(jù)庫中的已知毒性進(jìn)行比照,得出計(jì)算機(jī)預(yù)測的結(jié)果。最終結(jié)果顯示,利用計(jì)算機(jī)測試得到的毒性準(zhǔn)確率為87%,而使用動(dòng)物再次進(jìn)行測試的正確率僅為81%。這個(gè)結(jié)果從某種程度上揭示用計(jì)算機(jī)替代動(dòng)物試驗(yàn)的潛在可能性。此外,類器官芯片的發(fā)展也為動(dòng)物模型不足和動(dòng)物模型不能準(zhǔn)確預(yù)測人體反應(yīng)提供了解決方案。類器官芯片因?yàn)槭侵苯永萌祟惤M織構(gòu)建,且可定制化為疾病建模;因此可以在臨床試驗(yàn)前更充分的進(jìn)行效價(jià)評估,將不合適的藥物排除,從而提升藥物研發(fā)成功率,降低后期藥物開發(fā)成本且減少動(dòng)物傷害。此外,類器官芯片和AI技術(shù)的融合也將使非動(dòng)物性體內(nèi)藥物篩選更高效和精準(zhǔn)。雖然人工智能和類器官等新技術(shù)的應(yīng)用將帶來了全新的研發(fā)思路,但目前仍有很多不定因素和未知困難。首先是數(shù)據(jù)整理問題,用于安全性測試的數(shù)據(jù)需要長達(dá)數(shù)年的累積,然后是數(shù)據(jù)的清洗和整理。其次,動(dòng)物試驗(yàn)本身也有計(jì)算機(jī)推測難以比擬的優(yōu)勢。臨床前藥理/毒理實(shí)驗(yàn)中,我們之所以會(huì)選用在生理特征上與人類相似的動(dòng)物來進(jìn)行,是因?yàn)槿梭w組成非常復(fù)雜,許多的副作用、機(jī)體反應(yīng)、過敏,往往是在實(shí)驗(yàn)室中無法預(yù)測的,而使用動(dòng)物則更容易讓我們預(yù)測試驗(yàn)藥品在人類體內(nèi)的各種反應(yīng)。類器官存在異質(zhì)性問題,比如干細(xì)胞可能取自不同的個(gè)體,培養(yǎng)出來的類器官在大小、形狀和細(xì)胞成分方面都是異質(zhì)的(某些特征存在差異);不僅如此,盡管某些干細(xì)胞取自同一個(gè)個(gè)體、培養(yǎng)在同一個(gè)實(shí)驗(yàn)室,都會(huì)出現(xiàn)這種異質(zhì)性。削減動(dòng)物試驗(yàn)還有很長的路要走雖然已經(jīng)出現(xiàn)了一系列潛在的動(dòng)物試驗(yàn)替代技術(shù),但我們應(yīng)該看到,目前我們所擁有的這些替代技術(shù)還不足以讓人類放棄各種動(dòng)物試驗(yàn)。為此,我們采訪了深圳埃格林醫(yī)藥的杜濤博士。杜博士是FDA的前審評官員,也是一位在臨床前研究和早期臨床試驗(yàn)方面很有造詣的科學(xué)家。杜博士指出,新出臺的《FDA現(xiàn)代化法案2.0》更像一個(gè)催化劑,鼓勵(lì)藥企在新藥研發(fā)中盡可能地限制動(dòng)物試驗(yàn),但目前大幅度的削減動(dòng)物試驗(yàn)仍然是不現(xiàn)實(shí)的。“即使美國參眾兩院都通過了上述法案,F(xiàn)DA仍需要至少1-2年的時(shí)間去出臺一系列包含各種執(zhí)行細(xì)節(jié)的指導(dǎo)文件,而世界各國也不會(huì)立刻就會(huì)跟著FDA去限制實(shí)驗(yàn)動(dòng)物的使用。”杜濤博士回應(yīng)道。我們應(yīng)該看到,無論從倫理上、技術(shù)上和成本上,我們必須在減少實(shí)驗(yàn)動(dòng)物的使用。這對全球醫(yī)藥工業(yè)即是技術(shù)上的挑戰(zhàn),也是新的商機(jī)。減少動(dòng)物使用雖然是未來必須要做到的,但目前我們?nèi)孕璋凑宅F(xiàn)有法規(guī)去開展的臨床前藥理/毒理實(shí)驗(yàn)。“我相信,隨著AI技術(shù)的不斷成熟和替代技術(shù)的不斷完善,未來將會(huì)出現(xiàn)很多可靠的無動(dòng)物藥理/毒理檢測方法”。杜濤博士補(bǔ)充說。